Câu 1. Trong tự nhiên brom có hai đồng vị, đồng vị 79Br chiếm 54% số nguyên tử và nguyên tử khối trung bình của brom là 79,92. Xem nguyên tử khối có giá trị bằng số khối thì đồng vị thứ hai có số khối là
A. 82. B. 83.
C. 80. D. 81.
Trong tự nhiên kali gồm 3 đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của 39K trong KBr là
A. 30,56%.
B. 29,92%.
C. 31,03%.
D. 30,55%.
Đáp án D
%41K = 100 - 93,26 - 0,012 = 6,728%.
Khối lượng nguyên tử trung bình của K là:
MK = 39 x 0,9326 + 40 x 0,00012 + 41 x 0,06728 = 39,13468.
Khối lượng nguyên tử trung bình của Br là:
MBr = 79,92.
Thành phần phần trăm của 39K trong KBr là
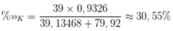
Trong tự nhiên Brom có 2 đồng vị bền: 79Br chiếm 50,69% số nguyên tử và 81Br chiếm 49,31% số nguyên tử. Hãy tìm nguyên tử khối trung bình của brom.
Nguyên tử khối của Brom là :
\(\overline{A}=\frac{79.50,69+81.49,31}{100}\approx79,98u\)
Vậy Nguyên tử khối trung bình của Brom là \(79,98u\)
Nguyên tử khối trung bình của Br là:
\(\overline{A}=\frac{79.50,69+81.49,31}{50,69+49,31}=\frac{7998,62}{100}=79,9862\)
Vậy nguyên tử khối trung bình của Br là 79,9862
Mọi người giúp e với..Mai kiểm tra r
A/nguyên tử khối trung bình của nguyên tố Brom là 79,92%.trong tự nhiên ,nguyên tố Brom có hai đồng vị.biết(số khối 79,số hiệu nguyên tử 35 Br)chiếm 54%.tìm số khối A của đồng vị thứ 2
B/cho một sừng dịch chứa 8,19g muối NaX(X là halogen)tác dụng với một lượng dư AgNo3 thu được 20,09 kết tủa .Hãy tìm nguyên tử khối của X.
Brom có 2 đồng vị là 79br và71br Nguyên tử khối trung bình của Brom là 79,91. a) Tính % số nguyên tử mỗi đồng vị của Brom? b) Tính % khối lượng của79Br trong hợp chất CaBr2 (cho Ca = 40) ? c) Biết đồng vị 79Br có số hạt mang điện nhiều hơn số hạt không mang điện là 26 hạt. Xác định số hiệu nguyên tử của Brom ?
\(a.Đặt:\%^{79}Br=a\left(a>0\right)\\ \Rightarrow \%^{81}Br=100\%-a\\ \overline{NTK}_{Br}=79,91\\ \Leftrightarrow79a+81.\left(100\%-a\right)=79,91\\ \Leftrightarrow a=54,5\%\\ \Rightarrow\%^{79}Br=54,5\%;\%^{81}Br=45,5\%\)
b. Phần trăm theo KL đồng vị 79Br trong phân tử CaBr2:
\(54,5\%.\dfrac{70.91.2}{79,91.2+40}\approx43,59\%\)
c.
\(\left\{{}\begin{matrix}P=E\\P+N=79\\\left(P+E\right)-N=26\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P+N=79\\2P-N=26\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=35\\N=44\end{matrix}\right.\)
Brom trong tự nhiên là hỗn hợp 2 đồng vị: đồng vị 1 có số khối 79 chiếm 50,7% ; đồng vị 2 có số khối 81 chiếm 49,3%. Tính nguyên tử khối trung bình của brom.
Nguyên tử khối trung bình:
\(\overline{A}=\dfrac{50,7\cdot79+49,3\cdot81}{100}=79,986\approx80\)
Nguyên tử khối trung bình của Brom là 79.91. Brom có 2 đồng vị, trong đó đồng vị ⁷⁹Br chiếm 54.5% số nguyên tử.
a) Tính nguyên tử khối của đồng vị còn lại
b) Tính % khối lượng của đồng vị ⁷⁹Br có trong phân tử HBrO4
Biết trong tự nhiên Brom có 2 đồng vị là Br và Br, nguyên tử khối trung bình của Br là 79,91. Tìm số nguyên tử của từng đồng vị trong tổng số 4000 nguyên tử Brom?
Nguyên tử khối trung bình của brom là 79,91. Brom có 2 đồng vị biết 79br và 80br. Thành phần phần trăm số nguyên tử của hai đồng vị trên lần lượt là: a) 91% và 9%. b) 55,5% và 45,5% c)60% và 40%. d) 30% và 70%
Gọi phần trăm số đồng vị của 79Br và 80Br lần lượt là a,b
Ta có :
$a + b = 100\%$ và $ 79a + 80b = 79,91$
Suy ra a = 9% ; b = 91%
Chọn đáp án A
Trong tự nhiên nguyên tố Brom có 2 đồng vị là 3579 Br và 8135 Br Biết nguyên tử khối trung bình của Br là 79,91.
Tính số nguyên tử của mỗi đồng vị khi có 10 nguyên tử brom.